
ENLACE COVALENTE POLAR
|
|
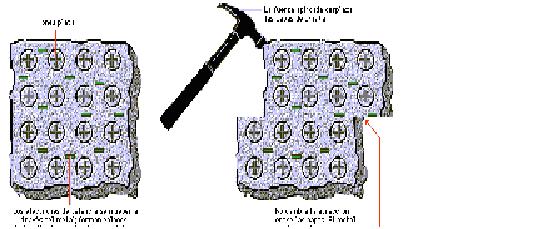
TIPOS DE ENLACE
|
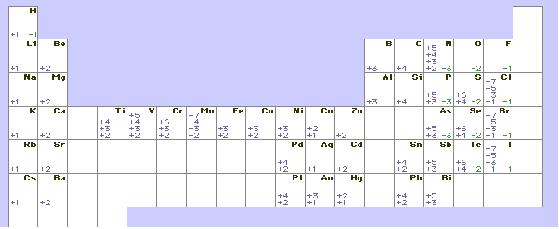
El simbolo suele representar un atomo del elemento. Sin embargo, los átomos tienen unas masas fijas, denominadas masas atómicas relativas, así que los símbolos representan a menudo una masa atómica del elemento o mol
|
|
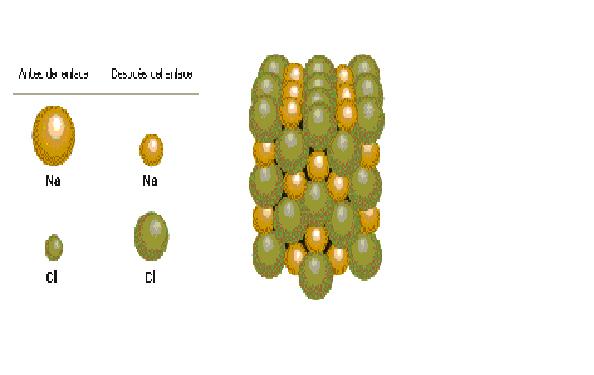 El enlace entre los átomos en la sal común (cloruro de sodio) es un típico enlace iónico
El enlace entre los átomos en la sal común (cloruro de sodio) es un típico enlace iónico
|
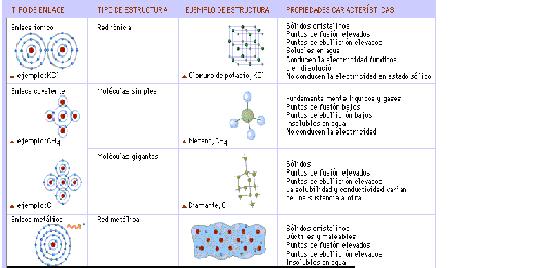
TIPOS DE ENLACES Y PROPIEDADESEl comportamiento químico de los sólidos, líquidos y gases que nos rodean está determinado por las formas en que los átomos se unen entre sí, lo que a su vez depende de las interacciones entre sus electrones más externos. Los electrones pueden transferirse de un átomo a otro (enlace iónico), compartirse entre átomos vecinos (enlace covalente) o moverse libremente de átomo en átomo (enlace metálico).
|
|
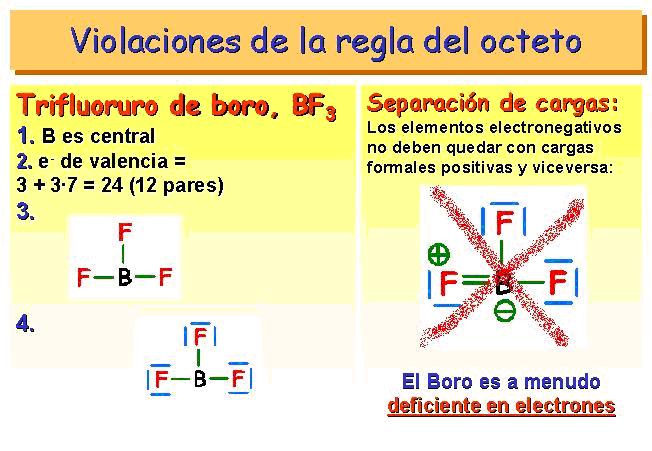
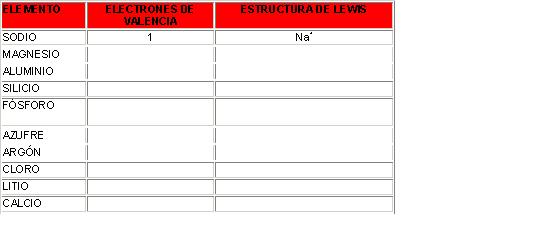 Parámetros a considerar en una estructura de Lewis
Parámetros a considerar en una estructura de Lewis
|

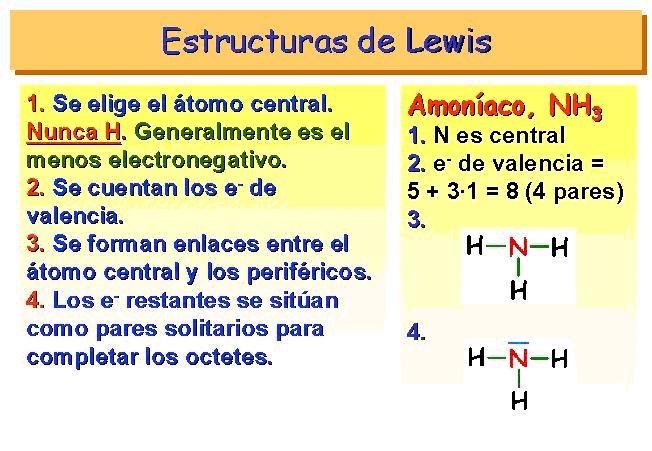
Gilbert Newton Lewis (1875-1946): Físico y químico norteamericano. Se le debe el estudio de los electrones periféricos de los átomos, del que dedujo, en 1916, una interpretación de la covalencia; propuso, en 1926, el nombre de "fotón" para el cuanto de energía radiante.
|
|
|
|
|
|
|
|
 Photo: My football accolades
Photo: My football accolades
|
|
|
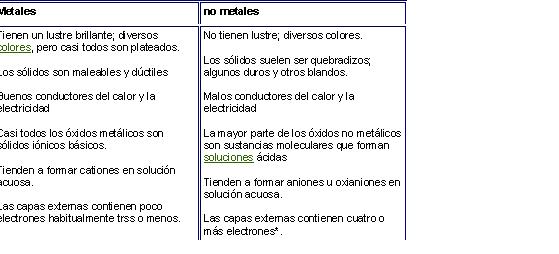
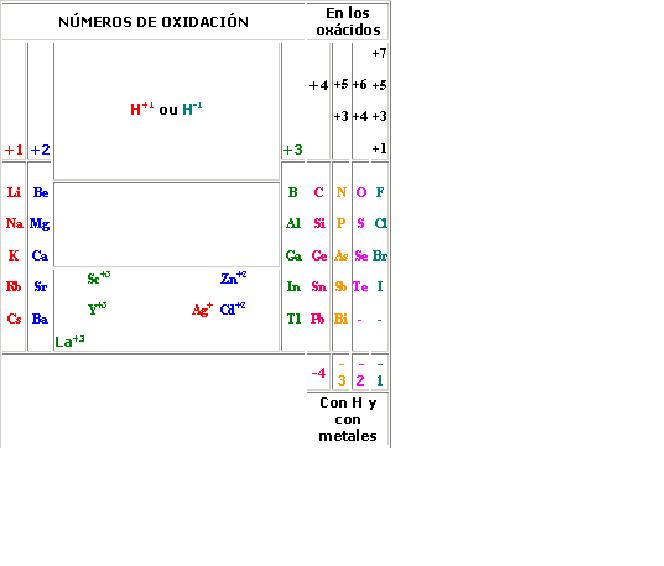
Comparación DE LOS METALES Y NO METALES
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|